Innere Medizin kk: COPD
《》Zurück zur Übersicht
Das Wichtigste
Bearbeiten- COPD ist ein englisches Wort und heißt chronic obstructive pulmonary disease = Chronisch obstruktive Lungenerkrankung
- Die COPD ist eine wichtige, häufige und chronische Lungenerkrankung, die überwiegend durch inhalative Noxen entsteht
- Typisch ist eine behinderte Ausatmung = expiratorische Obstruktion
- Eine Obstruktion ist eine Verengung der Atemwege oder ein erhöhter Atemwegswiderstand
- Der COPD zu Grunde liegt eine Entzündung der kleinen Atemwege und damit einhergehende Umbauprozesse im Lungengewebe, welche zu einer chronischen (obstruktive) Bronchitis und/oder einem Lungenemphysem führen
- Symptome sind pfeifende (Aus-)Atmung, Husten, vermehrter Auswurf, Atemnot bei Belastung sowie häufige Entzündungen der Atemwege.
- Eine Exazerbation ( = Verschlechterung) ist ein akute Zunahme der Symptome meist auf dem Boden eines Infektes
Krankheitsnummer ICD Klassifikation
BearbeitenICD-10
BearbeitenJ44.0 Chronische obstruktive Lungenkrankheit mit akuter Infektion der unteren Atemwege J44.1 Chronische obstruktive Lungenkrankheit mit akuter Exazerbation, nicht näher bezeichnet J44.8 Sonstige näher bezeichnete chronische obstruktive Lungenkrankheit Chronische Bronchitis: asthmatisch (obstruktiv) – emphysematös – obstruktiv J44.9 Chronische obstruktive Lungenkrankheit, nicht näher bezeichnet
Definition, englische Bezeichnung und Abkürzungen
Bearbeiten- Eine chronische Bronchitis liegt gemäß der WHO-Definition vor, wenn Husten und Auswurf in zwei aufeinanderfolgenden Jahren für jeweils mindestens drei Monate auftreten.
- Eine chronisch-obstruktive Bronchitis (COPD) bezeichnet darüber hinaus eine nicht bzw nur teilweise reversible Einschränkung des Atemflusses durch eine andauernde Entzündung der Bronchiolen. Im Gegensatz zur chronischen Bronchitis ist der Verlauf der COPD häufig progredient und mit letztendlich erheblichen extrapulmonalen Auswirkungen.
- Im Gegensatz dazu Asthma: reversible Obstruktion durch Bronchospasmolytika
- ACOS = ASthma COPD Overlap-Syndrom: Schnittmenge mit Erfüllung von Kriterien beider Krankheiten
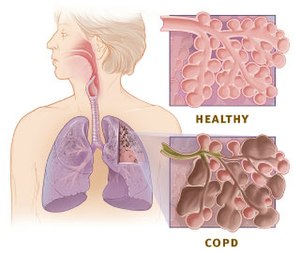
- besondere Verlaufsform der chronischen/chronisch obstruktiven Bronchitis Lungenemphysem: eine irreversible Zerstörung des Lungengerüsts und der Kapillaren, was zur Überblähung der Alveolen und einem vermindertem Gasaustausch führt.
- Exacerbation: akute Verschlechterung mit Zunahme Dyspnoe, Auswurfmenge und Änderung der Farbe des Auswurfs
Epidemiologie Statistik Kosten
Bearbeiten- Weltweit
- laut WHO waren 2016 251 Millionen Menschen an COPD erkrankt waren.
- Raucher/Ex-Raucher sind wesentlich häufiger betroffen als Nichtraucher, ebenso andere Formen der Innenraum-Luftverschmutzung, z.b. Kochen am offenen Feuer
- 2016 dritthäufigste Todesursache weltweit, besonders in Ländern mit niedrigem und mittlerem Einkommen (90 Prozent der weltweiten Tode durch COPD in diesen Länder)
- Deutschland
- 2010 c.a. 6,8 Millionen COPD-Erkrankte
- 12- Monats-Prävalenz 2017 bei > 18 Jährigen gesamt 5,8 Prozent (Männer und Frauen c.a. gleich verteilt), jedoch altersabhängig deutlich ansteigende Häufigkeit ( bei über 65 Jahren 11 bzw 12,5 Prozent)
- auch in Deutschland dritthäufigste Todesursache
Kosten
Bearbeiten- direkt als Behandlungskosten
- indirekt → Hauptlast durch Arbeitsausfall und vorzeitigen Ruhestand
- COSYCONET-Studie 2016:
- Häufigkeit der Arztbesuche bei COPD-Patienten doppelt so hoch bei gesunder Kontrollgruppe, unabhängig vom Schweregrad
- GOLD 1 jährliche Krankheitskosten um Faktor 2,5 erhöht, v.a. durch Medikamente, jährl. gerundet 4.400 EUR
- GOLD 4 um Faktor 5,7, v.a. durch Krankenhausbehandlungskosten, c.a. 10.700 EUR
- Häufigkeit der Arztbesuche bei COPD-Patienten doppelt so hoch bei gesunder Kontrollgruppe, unabhängig vom Schweregrad
- Zahl im Krankenhaus verbrachter Tage und der Arbeitsunfähigkeitstage bei COPD-Patienten deutlich erhöht
- 35-72 Prozent der COPD-Patienten gingen in vorgezogenen Ruhestand (vs. 15 Prozent der Gesunden), je nach Schweregrad
- c.a. 14.800 (GOLD 1) bis 33.800 EUR (GOLD 4)
Überschlagen müsste eine Packung Zigaretten bei der aktuell verkauften Menge /Jahr mindestens 40 Euro kosten, um die direkten und indirekten Kosten des Rauchens in Deutschland (Bronchial-Ca, COPD etc) zu decken. Dies würde sich natürlich dynamisch verändern, je nach dem wie viele Menschen rauchen und wie viele Zigaretten verkauft werden.
Ätiologie Ursachen
Bearbeiten- Rauchinhalation jeglicher Art, auch passiv
- Zigaretten (ab ca. 20–30 Pack Years sind 80-90% von einer chronischen Bronchitis betroffen), Pfeifen, Wasserpfeifen, Cannabis-Rauchmittel...
- offenes Feuer, Luftverschmutzung und Feinstaubbelastung
- organische und anorganische Stäube
- Steinkohleabbau, Schweißen, Umgang mit Mineralfasern oder quarzhaltigen oder chemischen Dämpfen
- rezidivierende bronchopulmonale Infekte sind Risikofaktor und Beschleuniger der Erkrankung
- fehlende 'normale' Entwicklung der Lunge in der Kindheit
- Tuberkulose
- Nikotinabusus der Mutter in Schwangerschaft
- fehlende 'normale' Entwicklung der Lunge in der Kindheit
- besondere Grunderkrankungen mit pulmonaler Beteiligung
- α1-Antitrypsin-Mangel
- Antikörpermangelsyndrome (z.B. IgA-Mangel)
- Ziliendyskinesie (z.B. Kartagener-Syndroms)
- Frühgeburt
- Punktmutationen für Tumor-Nekrose-Faktor (TNF) oder Mutationen im Gen MMP12 für eine Matrix Metallopeptidase bzw Makrophagen-Elastase,
Pathophysiologie und Pathologie
BearbeitenInhalative Noxen führen besonders in den Bronchioli zu einer Entzündung. Hält die Exposition an, kommt es durch fehlregulierte Schutzmechanismen und oxidativem Stress zu verschiedenen Veränderungen der Schleimhaut:
- Frühzeichen:
- Ansammlung von mononukleären Zellen in der Schleimhaut
- Hyperplasie und -trophi Schleimdrüsen und Becherzellen
- Verbreiterung der Basalmemran und Hypertrophie glatter Muskelzellen
- Zerstörung des Flimmerepithels
- Später:
- Schwäche der elastischen Verankerung der Bronchienwände ⇒ Kollaps der kleinen Atemwege bei forcierter Expiration, später auch größere Atemwege betroffen ⇒ permanente Druckerhöhung in der Lunge ⇒ Emphysem
- durch Reparatur Proteasen-/Proteaseninhibitor-Gleichgewicht zugunsten der Proteasen verschoben ⇒ Emphysem begünstigt
- Fibrosierung mit Narbenzügen, Zerstörungen der Alveolenwände und Kapillaren
- Umbau der Schleimhaut zu Plattenepithel
- schnelleres und pathologisches Altern der Lunge
- Kolonisierung mit Bakterien bei beeinträchtigter lokaler Abwehr ⇒ Verschlimmerung der chronischen Entzündung
- wichtige Zellen, die beteiligt sind
- ILC2-Lymphozyten
- Folgen:
- Instabilität der Bronchien v.a. bei forcierter Exspiration ⇒ Bronchialkollaps
- FEV1 i.e. Einsekundenausatemkapazität nimmt ab, exp. Spitzenfluss reduziert und expiratorische Flüsse bei Emphysem plötzlich schwer vermindert ⟨„Emphysemknick“ in der Fluss-Volumenkurve⟩
- Atemwegswiderstand besonders in der Expirationsphase erhöht ⇒ Golfschlägerartige Verformung der Resistanceschleife
- Parenchymverlust der Alveolen ⇒ schlechterer Gasaustausch und fortschreitendene Überblähung
- Zerchfelltiefstand, Wölbung Brustkorb und Sternum, Rippenhorizontalisierung
- Atemzugvolumen und Vitalkapazität vermindert zugunsten des Residualvolumens
- Intrathorakales Gasvolumen nimmt zu
- vermehrte Schleimproduktion bei erschwerter Expektoration
- Zunahme der Überblähung bei Anstrengung ⇒ kardiopulmonale Leistungsfähigkeit↓ ⇒ verstärkte Atemarbeit ⇒ Kachexie
- Instabilität der Bronchien v.a. bei forcierter Exspiration ⇒ Bronchialkollaps
Symptome und Klinik
Bearbeiten- chronischer Husten
- zunächst Morgens, später ganztägig
- weißlich zähes Sekret, morgens oft mukopurulent
- Belastungs-Dyspnoe
- langsame Zunahme von NYHA II bis IV bzw. nach mMRC
mMRC
Grad 1 Grad 2 Grad 3 Grad 4
Dyspnoe bei Eile oder Laufen nach Ankleiden
Hügel/Anstieg in der max. ⇒ kann
Ebene 90m kaum das
⇒ läuft ⇒ muss Haus
langsamer anhalten verlassen
als Gleich-
altrige
Grad 0
starker Anstrengung
- Spätzeichen
- Fassthorax
- Kopfschmerzen v.a. morgens a.e. durch CO2-Anstieg
- Plethora i.e. Gesichtröte durch Polyglobulie durch chroniche Hypoxie
- pulmonale Kachexie
Komorbiditäten
Bearbeiten- kardiovaskuläre Krankheiten (Schlaganfälle, Herzinfarkte, Herzinsuffizienz...)
- Diabetes
- Angsterkrankungen
- Depressionen
- Osteoporose
Diagnostik
BearbeitenBei der Diagnostik ist (ähnlich wie bei der Therapie) zwischen Erst-Diagnose, Verlaufskontrolle und Diagnostik in der Exacerbation zu trennen. Unten Genanntes ist beliebig erweiterbar und kann gerne als Leitfaden oder Checkliste genutzt werden.
- Erstdiagnostik: Ziel = Diagnosesicherung, Schweregrad für Planung erste Therapie, Komorbiditäten und Ausschluss Differentialdiagnosen
- Anamnese, körperliche Untersuchung und Vitalparameter
- internsitisches Routine-Labor inklusive ggf Genetik (e.g. a1-Antitrypsin-Mangel)
- Röntgen-Bild (als Ausgangswert), ggf HR-CT (High-resolution-CT)
- Komorbiditäten-erfassn
- ggf Echo (Rechtsherzbelastung? Linksherzinsuffizienz)
- Lungenfunktion inklusive Spasmolyse
- ggf TLCO bei Hypoxie
- Verlaufskontrolle: Ziel = Therapie-Evaluation, Komplikationen und Folgekrankehiten frühzeitig erkennen
- problembezogene Anamnese, körperliche Untersuchung und Vitalwerte
- Alltags-Symptome? körperliches Training? Infektionsprophylaxe? Ernährung?
- Häufigkeit von Exazerbationen und Stationäre notfallmäßige Behandlungen wegen COPD
- Therapieverträglichkeit und -wirkung, Selbstmedikation (!!sehr wichtig!!)
- Komorbiditäten: Herzkreislauf-, Krebs- und Osteoporoserisiko?
- (weiterer) Schulungsbedarf? Tabakentwöhnungsprogramm? Rehabilitationsbedarf?
- Lungenfunktion insbesondere FEV1 (alle 6-12 Monate) unter Dauertherapie aber vor Spasmolyse
- problembezogene Anamnese, körperliche Untersuchung und Vitalwerte
▷ o.g. am besten im Rahmen eines Disease-Management-Programme beim Hausarzt oder bei regelmäßigen Facharzt-Besuchen
- Diagnostik bei Exacerbation: Ziel = Infekt/nicht-Infekt-bedingt? Schwere? ⇒ Behandlungsplan
- Anamnese, körperliche Untersuchung und Vitalparameter
- Labor (v.a. Entzündungswerte, Hb), (kapilläre bzw arterielle) BGA
- Mikrobiologie: Blutkulturen bei Fieber, ggf Sputum/BAL
- Bildgebung: Röntgen/CT; Sono Lunge/Pleura
- Lungenfunktion (erst gegen Ende der Exacerbation, sonst verfälscht und zu schlecht)
Anamnese
BearbeitenWie immer das A und O eines Arztes, hier einige wichtige Eckpunkte:
- Alter bei ED/bei ED Risikofaktoren (v.a. Berufsanamnese und Pack years vs Lungenentwicklung gestört? bei ED-Alter ≤ 50 Jahre α1-Antitrypsin)
- Rezidivierende Infektionen der Atemwege
- Impfstatus
- Symptomschwere erfassen
- mMRC = Schwere der Dyspnoe
Grad ≤ 1 ≥ 2 GOLD A bzw C B bzw D https://www.mdcalc.com/mmrc-modified-medical-research-council-dyspnea-scale
- CAT = Quantifizierung Symptomatik und Erfolgskontrolle der Therapie in Form von Punktwerten (0–40)
Punkte ≤ 10 > 10 ≥20 GOLD A bzw C B bzw D schwere Symptome https://www.catestonline.org/patient-site-test-page-german-germany.html
- weitere: Kopfschmerzen, Tagesmüdigkeit? Depressionssymptome? Gewichtsverlust? Ödeme, kardiale Symptome?
- Exacerbations-Zeichen
- purulentes/vermehrtes Sputum
- Zunaghme Husten/Dyspnoe
- Exacerbationshäufigkeit
≤ 1x ambulant vs. ≥1 x Stationär oder ≥2x ambulant GOLD A bzw B C bzw D
- Differentialdiagnosen und Komorbiditäten abfragen
- Asthma? Allergien? Polyposis Nasi? Sinusitis?
- Schlafbezogene Atemstörungen
- Herz/Nieren- oder Lebererkrankungen
- Lungenkrebs? ⇒ bald wird ein CT-Thorax zum Screening empfohlen
- Angsterkrankung? Depression?
- zwei-Fragen-Test:
Fühlten Sie sich im letzten Monat häufig niedergeschlagen, traurig bedrückt oder hoffnungslos? Hatten Sie im letzten Monat deutlich weniger Lust und Freude an Dingen, die Sie sonst gerne tun?
klinische Untersuchung
Bearbeiten- Auskultation und Perkussion:
stabile COPD Exacerbation Emphysem
vesikuläres AG exp. Giemen abgeschwächtes AG
/Brummen bis zu Silent Lung
bei Infiltrat:
Rasselgeräusche
Zwerchfelltiefstand
Hypersonorer Klopfschall
- spätere klinische Zeichen:
- Zyanose zentral
- Einsatz Atem-Hilfsmuskulatur
- Rechtsherzinsuffizienz-Zeichen: Stauung Halsgefäße, Beinödeme...
bei langjähriger Hypoxie
- Uhrglasnägel, Trommelschlägelfinger
- Fassthorax
- Kachexie
- klinische Stereotypen
- pink puffer =
- blue bloater =
Labor
Bearbeiten- Blutbild inkl. DiffBB, CRP und ggf Procalcitonin
- Entzündungswerte? Wenn ja eher wegweisend für bakteriellen oder viralen Infekt?
viral/atypisch bakteriell:
Leukozyten Lymphozyten Neutrophile Procalcitonin
normal/erniedrigt erhöht/erniedrigt normal negativ
typisch Bakteriell:
Leukozyten Lymphozyten Neutrophile Procalcitonin
erhöht normal erhöht, normal/bei
Linksverschiebung l schweren Infektionen
erhöht
CRP ist unspezifisch und nur ein Parameter für die Ausprägung der Entzündungsreaktion
sowie zur Verlaufskontrolle.
- Hämoglobin ⇒ Hinweise für chronische Hypoxie bei Polyglobulie?
- Immunglobuline und Eosinophile:
- IgE gesamt: Spiegel-Erhöhung spricht für allergische Diathese (v.a. bei Asthma-COPD-Overlap interessant)
- Eosinophile im DiffBB: >300/nl spricht für relevantes entzündliches Geschehen (v.a. bei Asthma-COPD-Overlap interessant) --> Indikation für Glukocortikoide in Dauertherapie
- Antitrypsin
- Wann: bei Erstmanifestation < 50.LJ. ; bei Nichtrauchern
- Wie?
- Serumelektrophorese = Suchtest: bei schwacher oder fehlender a1-Globulinbande (<2g/l) Mangel wahrscheinlich (a1-Antitrypsin = 80% der a1-Globuline)
- Alpha-1-Antitrypsin im Serum (Fremdlabor), quantitativ als Bestätigung
- des Weiteren Phänotypisierung und Genotypisierung möglich
Mikrobiologie
BearbeitenBei Fieber und/oder hohen Entzündungswerten und/oder klarem Infiltrat im Röntgen
- Blutkultur
- Abstrichprobe aus dem Atemwegstrakt zum Screening gegenüber den häufigsten Erregern für Atmwegsinfekte (mindestens jedoch Influenza-A-, B- sowie Covid-Schnelltests)
- Urin-Antigentests auf Pneumokokken und Legionellen bei Pneumonie
Bei Unsicherheit bezüglich der Frage, ob ein Antibiotikum eingesetzt werden sollte, kann eine
- Sputum-Diagnostik
erfolgen. Genug Sputum ist ja meist vorhanden, vor Gewinnung ggf mit 3%-NACL-Lösung inhalieren lassen, dann ist die Expektoration leichter für den Patienten.
Sputum: 1) Zytologie Infekt-Exacerbation Nicht-Infekt-bedingt Neutrophilendominantes Bild Makrophagen-Dominanz ggf intrazelluläre Bakterien 2) Erregerdiagnostik mittels Kultur
Alle 1-2 Jahre wird auch routinemäßg eine Sputumkultur empfholen, um eine Keimbesiedleung bzw. einen Keimwechsel sowie Antibiotikaresistenzen zu erkennen.
- BAL
EKG
BearbeitenVorwiegend zum Ausschluss kardiogener abwendbarer gefährlicher Ursachen von Dyspnoe (STEMI, NSTEMI, tachykardes Vorhofflimmern...) sowie evtl. zum Erkennen von Rechtsherzbelastungszeichen (P-dextrokardiale, RSB (inkomplett oder komplett), Steil- oder Sagittaltyp beim älteren und/oder dicken Patient.
NB: supraventrikuläre (tachykarde) Rhythmusstörungen treten häufig assoziiert mit COPD auf, Vorhofflimmern/-Flattern etc. siehe entsprechendes Kapitel
Bildgebung
BearbeitenBei Dyspnoe je nach Auskultationsbefund:
- Sonografie
- Pleura: Erguss? wenn ja punktionswürdig? kompliziert/gekammert/Fibrinfäden?
- VCI: Rechtsherzbelastung? VCI- und Lebervenenstau? vs. Exsikkose?
- Lunge: Pneu? Pneumonie? Lungenödem?
NB: Lungensono wird tatsächlich nicht selten durchgeführt und ist weil nicht invasiv auch eine feine Sache, jedoch sieht man eben nur die randständigen Bereiche/die Lungenoberfläche
- Röntgen Thorax
Findet meist, in Form eines ap. Röntgen stehend in 2 Ebeneb bei akuter Verschlechterung statt, sowie bei Erstdiagnose. Verlaufskontrollen sind bei Symptomänderung oder Verdacht auf Carzinom sinnvoll.
- Befunde:
- Infiltrat? ⇒ bei Infektexacerbation, typisch vs atypisch vs V.a. Aspiration
- Atelektase? Mittellappensyndrom? ⇒ evtl. durch Tumorkompression?
- Pneu? ⇒ häufiger bei Bullae und Emphysem, Lage? Größe?
- pulmonalvenöse Stauung? Herzinsuffizienzzeichen?
- Pleuraerguss? Empyem? Schwarte?
- Neoplasie? primär/metastasiertes Tumorgeschehen?
- Kaverne?
- etc...
“typische COPD-Befunde”
- verdickte Bronchienwände, Deformation
- diffuse interstitielle Zeichnungsvermehrung
- Plattenatelektasen
- Emphysem (horizontalisierte Rippen mit vergrößertem Abstand, flaches Zwerchfell, Strahlentransparenz Parenchym↑, schmales Herz; setlich verbreiterter Durchmesser d. Thorax
- Ct-Thorax
- zur genaueren Abklärung unklarer Röntgenbefunde (Infiltrat? Covid-typisch? Carzinom? Aspergillose? TBC? Fibrose? Metastasen? Pneumothorax? Bronchiektasen bei häufigen Infekten? Emphysem +/- Bullae, ggf. vor einer operativen Resektion oder bei Verdacht auf akute vaskuläre Pathologien wie eine Lungenembolie, Hämatothorax, Empyem etc.
- bei Erstdiagnose, hier ein HR-CT
- weitere:
- Echo: In der Exacerbation orientierend ganz gut, bezüglich Komorbidität und ; Bei Erstdiagnose definitiv geraten als Ausgangswert sowie bei hohem KHK-Risiko
- Lungenszintigrafie: eher selten genutzt und nur in großen Häusern verfügbar; z.b. zusätzlich zu einem Nativ-CT bei v.a. Lungenembolie und Kontrastmittel-Kontraindikation sowie zur Planung vor Parenchymresektionen
speziell pulmonologische Diagnostik
BearbeitenGenerell ist zu unterscheiden, was man herausfinden will:
- Ist der Patient (aktuell/chronisch) respiratorisch insuffizient? ⇒ Screening Pulsoxymetrie
- Insuffzienz/V.a. Hyperkapnie:BGA arteriell oder kapillär
- Suffizienz: 6-min Gehtest zur Demaskierung einer latenten resp. Insuffizienz bei Belastung
- Liegt eine Obstruktion vor und/oder eine andere Ventilationsstörung? ⇒ Lungenfunktion (Spirometrie)
- Ist die Obstruktion fixiert? ⇒ Lungenfunktion (Spirometrie)mit Spasmolyse
- Liegt ein Emphysem vor? ⇒ Bodyplethysmografie
Des Weiteren:
- Diffusionsmessung bei Hypoxie
- Bronchoskopie bei schwerer Mukostase, Hämoptysen oder Aspiration, sowie bei Therapie-refraktärer Infektion oder v.a. atypsiche Erreger inklusive TBC und bei Tumorverdacht im CT
- Rechtsherzkatheter zur Quantifizierung und Differentialdiagnose einer pulmonalen Hypertonie
- Polysomnografie bei v.a. Schlafbezogene (obstruktive) Atemstörungen
BGA
BearbeitenWann, was und was sagt mir das? Hier eine kurze Zusammenfassung, ansonsten siehe Kapitel BGA:
- Wann?
- SpO2 <94-90%
- v.a. CO2-Retention
- starke Hyper/Hypoventilation
- Was:
arteriell kapillär ( venöse ) Information über Gasaustausch der Lunge (Gasaustausch des Gewebes)
▷ Zur Beurteilung der Lungenleistung sind nur kapillär oder arteriell wirklich aussagekräftig. Wenn das (zunächst) nicht geht, kann eine venöse BGA auch Aufschluss über eine respiratorische Azidose/Alkalose oder eine Hyperkapnie geben, ist aber durch das vorgeschaltete Kapillarbett nicht wirklich verlässlich.
- Was sagt mir das?
- Normoxämie:
Ziel-paO2 = 100 - (Lebensalter [Jahre] ÷ 3) Beispiel: 75-jähriger Ziel-PaO2 = 100- (75 ÷ 3) = 75mmHg
Alles über 100 bedeutet: 'Sauerstoff etwas zurückdrehen'.
- (Hypoxämische) Hypoxämie:
- Einteilung
- manifest (in Ruhe) vs latent (nur unter Belastung)
- leicht, moderat, mittelschwer und schwer
- Einteilung
▷ macht orientierend Sinn, es gibt aber keine universal gültigen Grenzwerte
- Normokapnie
pCO2 = 31-42mmHg
- Hyperkapnie > 45mmHg
- akut: PH-Verminderung ▷ Zeichen der gestörten Ventilation (und/oder Perfusion bei Lungenembolie); Atmungsunterstützung erwägen und Menge etwaiger Sauerstoffsubstitution wenn möglich reduzieren
- chronisch: PH normal, BE und HCO3 kompensatorisch erhöht (Basenretetion zur Elimination der 'Säure' CO2)
- Hypokapnie <30mmHg
- akut: eventuell mit PH-Verminderung, bei gesteigerter Atemfrequenz Zeichen der Hyperventilation; CAVE: irgendwann Erschöpfung möglich, Atemfrequenz jedoch der validere Parameter (> 25- 30/min streng überwachen!, > 30 Atmungsunterstützung erwägen)
- chronisch: eher selten, aber möglich
Lungenfunktion
BearbeitenEin Buch mit 7 Siegeln oder doch ganz leicht? Wie immer kann man es sich schwer oder leicht machen, hier die abgespeckte Variante für den erleichterten Zugang bezüglich der COPD:
- Liegt eine Obstruktion vor...?
- Fluss-Volumenkurve: mit vermindertem Spitzenfluss, Expiratorischer Teil abgeflacht
- expiratorische Flüsse (v.a. nach 25-50% der ausgeatmeten Vitalkapazität)
- ggf plötzlicher Druckabfall direkt nach Spitzenfluss bei forciertem Ausatmen v.a. beim Emphysem = 'Emphysem-Knick'
- Spirometrie:
- FEV1 < 100% des Solls (bezogen auf das Ideal je nach Größe, Geschlecht und Alter) und Tiffenau-Index < 70% nach Spasmolyse
- Fluss-Volumenkurve: mit vermindertem Spitzenfluss, Expiratorischer Teil abgeflacht
Die FEV1 (=Einsekunden-Ausatmungskapazität) ist relativ und absolut vermindert
- Fluss-Druck-Kurve: flussabhängige Obstruktion bei Ausatmung ⇒ 'Golf/Hockey-Schläger'-Deformation im expiratorischen Teil
- Bodysplethysmografie: Widerstand bei Ausatmung erhöht
- ...und wenn ja wie schwer?
- Spirometrie: quantitativ wie schwer vermindert die FEV1 ist
- Fluss-Druck-Kurve: je flacher die Achse desto stärker die Obstruktion, je Hockeyschlägerartiger desto schlimmer
- Ist die Obstruktion reversibel?
Signifikante Reversibilität bei Änderung der FEV1 nach Spasmolysegabe vollreversibel: FEV1 nach Spasmolyse mind. 200ml bzw. 12% mehr im Vergleich zum Ausgangswert teilreversibel: FEV1 verbessert nach Spasmolyse, aber < 200ml bzw. 12%
- Liegt eine Überblähung der Lunge vor...?
- akut/Pseudo im Sinne eines Volumen pulmonum auctum
- manifest im Sinn eines Emphysems
- Hier Schweregrad:
1 leicht FEV1 > 80 % d. Solls, 2 mittel 49 % < FEV1 < 80 % d.S. 3 schwer 30 % < FEV1 < 50 % d.S. 4 sehr schwer FEV1 < 31 % d.S.
Beispiel für Befundung:
mittelschwer verminderte expiratorische Flüsse und FEV1 ( X,X l ~ XX% d.S.) ohne signifikantes Ansprechen auf Bronchospasmolyse, sowie schwere Lungenüberblähung (TGV XX % d.S. bzw RV/TLC XX %).
Fehlerquellen:
- schlechte Mitarbeit: die Fluss-Volumenkurve muss geschlossen und halbwegs stimmig sein mit dem Ideal
- viel Sekret = viel Husten
- Exacerbation: mitten in der Exacerbation sind die Werte nicht aussagekräftig, es empfiehlt sich daher die Lungenfunktion erst gegen Ende des Aufenthalts zu machen, wenn es dem Patienten besser geht sowie im Intervall zu wiederholen, wenn keine Exacerbation vorliegt
6 Minuten Gehtest
BearbeitenPatient geht in 6 Minuten so schnell er kann, die Wegstrecke in Metern wird gemessen.
▷Essentiell für die Verordnung von Sauerstoff als Langzeittherapie zur Evaluation der benötigten Menge unter Belastung.
Einteilung Schweregrad
BearbeitenDie Einteilung der COPD nach GOLD, also nach FEV1, Symptomen und Exacerbationshäufigkeit ist für die Therapie entscheidend, ebenso die Unterscheidung einer irreversiblen vs. einer (teil)reversiblen Obstruktion.
Schweregrad nach GOLD
BearbeitenGlobal Initiative for Chronic Obstructive Lung Disease (GOLD) von 2007
Klinische/Symptomatische Einteilung der Schwere der COPD
GOLD C D Exacerbationen ≥1 Stationär/ ≥2 ambulant
A B Exacerbationen ≤ 1ambulant
≤ 10 CAT-Punkte ≥ 10 CAT-Punkte
bzw mMRC ≤1 bzw mMRC ≥2
Schweregrad nach FEV1
BearbeitenWird zunehmend zugunsten von GOLD weniger wichtig, aber durch gute Erfassbarkeit klinisch breit eingesetzt
Schwere nach FEV1 --------------------------------------------------------------------------------- 1 leicht FEV1 > 80 % Soll, FEV1/FVC < 70 % 2 mittel 49 % < FEV1 < 80 % Soll FEV1/FVC < 70 % 3 schwer 30 % < FEV1 < 50 % Soll FEV1/FVC < 70 % 4 sehr schwer FEV1 < 31 % Soll FEV1/FVC < 70 % oder FEV1 < 50 % Soll plus chronische respiratorische Insuffizienz
- FEV1 = forciertes exspiratorisches Volumen in der ersten Ausatmungssekunde = Einsekundenkapazität
- FVC = forcierte Vitalkapazität (siehe Lungenfunktion)
'klassische COPD' vs. Asthma-COPD-Overlap
BearbeitenBei einer COPD gilt es, eine asthmatische Komponente nachzuweisen/auszuschließen, da hier schon frühzeitig ein inhalatives Glukokrtikoid eingesetzt werden sollte. Ein ACOS liegt vor, wenn
- die Obstruktion signifikant (> 12% bzw 200ml) reversibel ist
- eine Eosinophilie im Sputum oder > 300/nl im Blut vorliegt.
klinische Stereotypen
BearbeitenNur der Vollständigekeit-halber erwähnt, therapeutisch nicht wirklich relevant:
- pink puffer = Emphysemtyp, kachektisch, Hypoxie vorherrschend
- blue bloater = Bronchitistyp, oft adipös, zyanotisch, Hyperkapnie vorherrschend
Therapie
BearbeitenWieder wichtige Unterscheidung Dauer/Intervalltherapie vs Exacerbation
Dauertherapie
BearbeitenBehandelt wird je nach Schweregrad im Sinne einer Kombination aus GOLD und FEV1, sowie abhängig davon, ob es sich um eine 'klassische' COPd oder um ein Asthma-COPD-Overlap handelt.
Gold A B C D
[FEV1 > 80%, [FEV1 80-50%, [FEV1 50-30 [FEV1 <30%/resp. insuff
geringe Symptome, viel Symptome, geringe Symptome viel Symptome
geringes Risiko] geringes Risiko] hohes Risiko] geringes Risiko]
Dauertherapie nicht Monotherapie Monotherapie LAMA LAMA + LABA
zwingend,evtl. Mono LAMA / Kombi LAMA + LABA bei Overlap:
LAMA oder LABA (LABA + ICS) LABA + ICS
(+/- LAMA)
SABA +/- SAMA bei Bedarf
Wichtig ist die regelmäßige udn korrekte Anwendung, siehe einzelne Kapitel zu den Medikamenten und Inhalatoren. Immer, wenn die Initialtherapie nicht zur Symptomkontrolle führt, trotz optimaler Anwendung und Compliance, ist eine Eskalation sinnvoll. Es gibt zur Erhöhung der Anwenderfreundlich keit 2er und 3er-Fixkombinationen aller Art zwischen LABA,LAMA und ICS.
Ab GOLD D können zusätzlich
- Roflumilast, ein Phosphidisterase-4-Hemmer
- Theophyllin, ein oraler ß-Agonist
Dosierung, Nebenwirkungen etc siehe dort.
Bei häufigen (> 2 Exacerbationen im JAhr) und dem Nachweis einer Pseudomonas aer.-Besiedelung sollte eine Dauertherapie mit einem Makrolid (z.b. Azithromycin) erwogen werden, Nachteil hierbei ist die Resistenz-Bildung insbesondere bei Pneumokokken, die bereits in einigen EU-Ländern zum Problem geworden ist.
Bei ACOS, also Asthma-COPD-Overlap-Syndrom kann ab Gold (B -) D bei schwerer Symptomatik ein inhalatives Steriod probiert werden. Bessern sich hierbei die Symptomatik und die Lungenfunktion, kann es weitergegeben werden. Ist jedoch nach einigen Wochen keine Besserung erkennbar, sollte das ICS wieder abgesetzt werden, da sich das Risiko für pulmonale Infekte erhöht, sprich das Kostn-Nutzen-Risiko wird ungünstig.
Mukolytika und Antitussiva
BearbeitenErstere können etwas nützen, manche Patienten profitieren jedoch nicht
- NACC
- z.b. 600mg als Brause 0-1-0
- Ambroxol
vs.
- Noscapin
- z.b. 20-25mg nachts
- Codein
- 30-50mg zur Nacht (maximal 48gtt 3x/d)
CAVE potentiell atemdepressiv Antitussiva am besten abends/nachts, da tagsüber abgehustet werden soll
'apparative' und 'operative' Therapie
BearbeitenBei chronischer respiratorischer Insuffizienz verschlechtert ich die Langzeitprognose des Patienten: die chronische Alveoläre Hypoventilation führt zu einer hypoxischen pulmonalen Vasokonstriktion (sog. Euler-Liljestrand-Mechanismus), dadurch werden die pulmonale Hypertonie und damit das Cor pulmonale hervorgerufen.
Es hat sich gezeigt, dass eine Langzeit-O2-Therapie bei hypoxischer bzw eine Heim-Beatmung bei hyperkapnischer Insuffizienz das Überleben durch eine Verhinderung bzw. Verzögerung dieses Mechanismus' bewirken können.
Langzeit-O2-Therapie
BearbeitenWenn eine dauerhafte Hypoxämie (pO2 in Ruhe 55mmHg), also COPD IV trotz optimaler sonstiger Therapie vorliegt bzw. in palliativer Indikation auch bei höheren Werten, ist eine Langzeit-Sauerstofftherapie (LTOT) zu Hause möglich (mindestens 16 Stunden täglich) Der Nutzen muss erwiesen sein, sprich der pO2 muss durch die Gabe ansteigen (palliativ: der Patient muss sich besser fühlen). Zudem darf der pCO2 nicht über Werte steigen, die der Körper kompensiert. Bei mobilen Patienten sollte immer zuerst ein Sauerstoffkonzentrator für zu Hause und Unterwegs (mobile Fomr mit Akku) und Triggerfunktion verordnet werden, dabei muss man testen, ob der Patient triggern kann (mit einem Testgerät und BGAs hierunter im Vgl zu O2 permanent.
Langfristig ist den O2-Firmen Flüssigsauerstoff meistens lieber, da sie den Tank regelmäßig befüllen kommen müssen und das mehr einbringt.
Neuerdings kann auch eine Highflow-Therapie für zu Hause verordnet werden, entweder bei Hypoxie und/oder Hyperkapnie. Daten hierzu gibt es noch nicht so viele wie für die Maskenbeatmung.
Heimbeatmung
BearbeitenIndiziert bei:
- (akut auf) chronischer Hyperkapnie (pCO2 >50 mmHg) sowie Ruhedyspnoe und ggf zentralnervösen Einschränkungen durch die Hyperkapnie.
zudem sinnvoll bei:
- sowie bei pulmonaler Kachexie durch hohe Atemarbeit
Es erfolgt eine nichtinvasive Beatmung über Nacht und in Ruhephasen tagsüber (mind 6-8h/d). Dadurch kommt es zu einer Erholung der Atemmuskulatur, sodass in den nicht-beatmeten Zeiten des Tages die Lungenleistung verbessert werden kann.
Neuerdings kann auch eine Highflow-Therapie für zu Hause verordnet werden, s.o.
Düsenvernebler bzw Inhalationsgerät
BearbeitenAtemtrainer, Cough-Assistant, Flutter oder Cornet-Systeme, IPPB
BearbeitenLungenvolumenresektion
BearbeitenEmphysematische Areale tragen nicht mehr zum funktionellen Gasaustausch bei und neigen im Gegenteil zu Komplikationen (Infekte, Pneu, Hämoptysen etc.). Sie können von der Ventilation abgekappt werden, wodurch sich die Überblähung verringert und sich Dyspnoe und Lungenfunktion verbessern können. Wichtig ist die korrekte Indikationsstellung mittels HRCT, Lungenfunktion und evtl Bronchoskopie
- Wann?
- bei therapirefraktärer Dyspnoe, resp. Insuffizienz, rezidivierenden Hämoptysen bzw. schwer sanierbaren rezidivierenden Infekten bei entsprechenden patho-anatomischen Voraussetzungen, sprich nicht generalisiertes Emphysem, sondern lokalisiertes Emphysem
- CAVE: FEV1 sollte noch > 20–25% sein, da sonst OP-Risiko zu hoch. Die operative Sterblichkeit ist generell hoch, der Gewinn an Lebensqualität ist schwer vorherzusagen.
▷Individuelle Entscheidung
- Endoskopisch: bronchoskopisches Einsetzen von Okklusions- oder Ventilsystemen in überblähte Lungenanteile
- operative Volumenreduktion
- Lungenteilresektion v.a. bei Oberlappenbetontem Emphysem (schlechtere Perfusion ohnehin im Stehen hier --> weniger Gasaustausch)
- Bullektomie (Bullae, die mehr als ⅓ eines Lungenflügels einnehmen und funktionierendes Lungengewebe dadurch behindern)
Lungentransplantation
Bearbeitenbei fortgeschrittener COPD mit Lungenemphysem und schwerster Diffusionsstörung bei
- Patienten <60J mit ansonsten guter Prognose
- Rauchabstinenz seit > 6 Monaten und einer schwerst verminderten FEV1 (<20–25%) + DLCO <20%
- Langzeit-Sauerstofftherapie oder Heimbeatmung
- und Pulmonale Hypertonier
weitere Maßnahmen bei chronischer Bronchitis
Bearbeiten- Nikotinkarenz am besten mittels Raucherentwöhnungsprogramm
- Impfungen gg. Lungenpathogene Erreger (Influenzaviren (jährlich), Pneumokokken-Impfung, Covid19)
- Patientenschulung v.a. bezüglich Notfallsituationen (Lippenbremse, Atemhilfsmuskulatur, Ruhe bewahren) und dauerhaft Atemtraining
- Sole-Inhalation mit 3%-NACL
Achtung: nicht dauerhaft zu Hause mit SABAs wie Salbutamol inhalieren lassen, da eine Reduktion/ein Absterben der Zillien des Flimmerepthels beobachtet wird
- Drainagelagerung auf allen Vieren
- tägliche körperliche Aktivität auf einem angepasstem Niveau
- Osteoporoseprophylaxe (Vitamin D3 und Calcium) v.a. bei häufigem Cortisoneinsatz
- Psychiatrische Komorbidität mitbehandeln (häufig!!!, Luftnot fördert Angst)
- Trizyklische-Antidepressiva wie Opipramol (Startdosis 50mg 1-3x tgl, v.a. Abends mehr Dosis als morgens, da Schläfrigkeit a.s NW, maximal 300mg/d)
- kognitive Verhaltenstherapie
keine serotonergen Antidepressiva! --> pulmonale Beschwerden
- Ernährungsoptimierung und ggf -beratung
- Ambulante oder stationäre Reha?
Exacerbation
BearbeitenJe nach Schwere und ob Infekt-bedingt oder nicht, s.o. Die Mehrzahl der Exacerbationen ist infektbedingt, häufige Erreger sind Haemophilus influenzae und Streptococcus pneumoniae, meist aber Viren, weswegen ein Antibiotikum nicht immer notwendig ist
Notfall-Management und -Therapie
BearbeitenErsteinschätzung (problembezogene Anamnese, klinische Untersuchung, Abwägung Differentialdiagnosen, Oxygenierung und Co2-Elimination = Beatmungsindikation prüfen)
- Sitzende Lagerung, mindestens ein sicherer i.v.-Zugang, Ohr mit Hyperämie-fördernder Salbe einreiben lassen für BGA
- Prednisolon 50-100mg i.v.
- Salbutamol und Atruvent vernebelt zum Einatmen geben
- parenterale Gabe ß-Mimetika
Kurzinfusion Theophyllin 200mg oder Reproterol 0,09mg (=1 Amp) als (mehrfache) Kurz- oder Dauerinfusion via Perfusor (maximal 3-4 d) 18 - 90 μg/h, entspricht 450µg/50ml (5 Amp., 9µg/ml) ⇒ Laufrate 2 max. 10ml/h, bzw 900µg/50ml (10 Amp., 18µg/ml) ⇒ Laufrate 1 max. 5ml/h Ausschleichen sonst Rebound-Effekt ( stufenweise über 6–24 h) ▷Achtung: nur unter Überwachung der Herzfrequenz! nicht > 150
- ggf Terbutalin = Bricanyl s.c. 0,25-0,5mg
- bei parallel Herzinsuffienz und gutem Blutdruck: Lasix 40mg i.v. (DK-Anlage erwägen)
- Beruhigen, ggf Anxiolyse jedoch mit möglichst wenig Atemdepression
- Midazolam mg-weise (start low!)
- Morphin auch nur sehr vorsichtig, wirkt nicht so gut anxiolytisch!
- Frequenzkontrolle bei supreventrikulärer Tachykardie (Hufig begleitend!)
- Verapamil bei guter LV-Funktion 5mg , ggf nach 10 min erneut
- Digitoxin 0,5mg bei normalem Kalium
- Magnesium 2g als Lurzinfusion, 5g über 5h in 500ml Nacl
Hier definitiv Furosemid dazu, außer bei Fieber!
häufige Differentialdiagnosen, auch überlappend:
- kardiale Dekompensation
- Lungenembolie
- Pneu, v.a. bei Bullae
Allgemein
BearbeitenAtmungsunterstützung akut ja oder nein? -> wenn ja NIV-Beatmung -> bei nicht reversibler Hyperkapnie unter Therapie Intubation -> zur Entwöhnung bzw bei bleibender Hyperkapnie Langzeit-Heimbeatmung, s.u.
Zusätzlich sollte jeder Patient
- Sauerstoff bei Bedarf erhalten
Achtung: Übertherapie und Hyperkapnie beachten Kontraindikation = gleichzeitig Rauchen, da Brandbeschleunigung Indikation für Dauertherapie streng prüfen ▷vorrübergehend evtl sinnvoll, aber auf lange Sicht notwendig?
- Inhalieren mit Nacl 3%, Salbutamol und/oder Atruvent 1-1-1-1
- den Volumenstatus optimieren bekommen (Substitution vs Entzug)
- Atemgymnastik +/- Vibraxmassagen und physikalische Therapie mit kaltem Wasser +/l heiße Rolle zur Sekretmobilisation erhalten
- inhalative Noxen meiden
- Dauertherapie evaluieren lassen
- Zeigen, wie Patient das einnimmt (Therapiefehler?)
- Erhebung des (aktuellen) GOLD-Stadiums und der FEV1 am Ende der Exaerbation
- ▷ggf Erweiterung/Umstellung
zudem nicht vergessen: Thromboseprophylaxe, ggf Magenschutz ufn Osteoporoseprophylaxe
(bakteriell) Infektbedingt
BearbeitenIndividuelle Anpassungen sind immer notwendig, hier nur eine kurze Auswahl
- Antibiotikum über 5-7d:
ambulant erworben: ▷ Ampicillin-Sulbactam +/- Clarithromycin oder Doxycyclin schwer bzw nosokomial bzw Frührezidiv bzw hohes Pseudomonasrisiko: ▷ Piperazillin-Tazobactam +/- Clarithromycin und/oder Levofloxacin bzw Ciprofloxacin (bei Psd-Verdacht und schwerem Verlauf)
Nicht-Infekt-bedingt bzw nach erfolgreicher Infektbehandlung
BearbeitenNiedrigdosiertes Cortisonschema, z.b.
Prednisolon 20-30mg über 3-5d bei schwerer Exacerbation langsam reduzieren
Nichtmedikamentöse supportive Maßnahmen bei Akuter Bronchitis
BearbeitenEs gibt eine Reihe von nicht medikamentösen Maßnahmen, die ein Patient mit einem Atemwegsinfekt als angenehm empfindet und die wahrscheinlich hilfreich sind. Bei der guten Spontanheilungsrate ist allerdings ein Wirkungsnachweis nur schwer zu führen. Brauchbare Aussagen erhält man von Patienten, die immer wieder unter Atemwegsinfekten zu leiden haben. Nach dem Ausprobieren der verschiedensten Möglichkeiten bleiben meistens drei oder vier Maßnahmen übrig, die diese Patienten als wirksam erachten:
- Kühle, feuchte und frische Luft
Da eine Entzündung der Atemwege vorliegt, wird kühle, feuchte und frische Luft als lindernd empfunden. Meistens schläft der Patient mit immer wieder auftretender Erkältung warm eingepackt bei offenem Fenster, es sei denn, es herrscht sehr kalte trockene Winterluft unter −10 Grad Celsius. Trockene, warme Luft wird als unangenehm betrachtet und gemieden. Zugluft wir als unangenehm empfunden. Die Empfindlichkeit gegenüber Luftschadstoffen wie beispielsweise Zigarettenrauch ist erhöht. Stichwort: Auf einen Sonnenbrand hält man auch keinen Heißlüfter
- Anpassung der Temperaturregulation
Im Rahmen deines Atemwegsinfektes herrscht ein Durcheinander der Temperaturregulation im Körper. Man kann gleichzeitig an den Füßen frieren und am Kopf schwitzen. Die Schwitzneigung ist generell verstärkt. Bereits bei geringer Anstrengung kommt man vermehrt ins Schwitzen, um kurz danach wieder zu frieren, da man mit verschwitzter Kleidung schnell friert. So muss man ständig in Sachen Temperaturregulation nachhelfen: Ist der Körper zu warm und verschwitzt, sollte man ihn kalt abwaschen und wieder trockene Kleidung anziehen. Friert man, dann sollte man sich warm anziehen, sich bewegen oder ins Bett legen, um die Körpertemperatur wieder anzuheben. Stichwort: Immer gegen die Berg-und Talbahn der Körpertemperatur ankämpfen.
- Kaltwasseranwendungen (Kneippsche Güsse)
Kurzfristig Kaltwasseranwendungen wie Arm-, Bein- oder Oberkörpergüsse führen zu einer Aktivierung des Leistungsnervs ( Sympathikus ), damit zu einer Abschwellung der Nasenhöhlen und Bronchien und werden meistens als angenehm und krankheitsverkürzend empfunden. Vorsicht ist geboten bei ansteigendem Fieber und bei bereits vorhandenen kalten Füssen oder Händen. Hier sollte man sich vor den kalten Güssen erst wieder komplett aufwärmen. Stichwort: Kurze Kälte ist gut, lange Kälte ist schlecht.
- Allzu lange Bettruhe ist zu vermeiden
Da man bei leichter Körperaktivität die Bronchien und Nasenhöhlen erweitert, besser Luft bekommt und besser abhustet, ist ein gemütlicher Spaziergang im Wald 2–3 mal täglich von etwa 30–60 Minuten Dauer wahrscheinlich besser als eine dauernde Bettruhe. Allerdings sollte dazu kein hohes Fieber vorliegen und der Kreislauf sollte nicht instabil sein. Man darf dabei nicht frieren, sondern muß warm angezogen sein. Stichwort: Lange Bettruhe macht krank.
- Nahrungsmittel, die im Rachen nicht reizen
Da bei einem Atemwegsinfekt meistens auch der Rachen mit entzündet ist, werden flüssige Nahrungsmittel wie Wasser und Milch, Apfelbrei und Joghurt als angenehm, hingegen bröselige, trockene oder auch salzige Nahrungsmittel als unangenehm empfunden. Jedes Verschlucken von Nahrungsmitteln in die Luftwege löst einen sehr unangenehmen Hustenanfall aus und sollte vermieden werden. Stichwort: Rachen mit Sahne ölen.
Wärme bei chronischer Bronchitis/Sinusitis mit morgendlicher Verschleimung und chronischem Husten
BearbeitenKurze Kältereize und frische Luft werden von den meisten Patienten mit akutem Atemwegsinfekt als lindernd empfunden.
Bei wochenlangem chronischen Husten und starker morgendlicher Verschleimung bei chronischer Bronchitis oder chronischer Sinusitis hilft die Kälte aber wohl nicht, sondern ist eher kontraproduktiv, vor allem wenn sie länger als ein paar Minuten einwirkt..
Man sollte dann auf jeden Fall einmal das Gegenteil probieren: Wärme
Die Wärme kann man zB durch tägliches 15 minütiges heißes Duschen, durch warme Getränke und durch warme Bekleidung zuführen bzw im Körper halten.
Auch indoor Bewegung zB auf dem Heimtrainer kann zur Erwärmung sehr hilfreich sein, solange Herz und Lunge das noch zulassen.
Die Wärme führt zu einer Öffnung der Hautgefäße und offensichtlich zu einer Umverteilung der Blutmenge aus der Lunge. Das führt auch zu einer Austrocknung bzw Schleimreduktion der Atemwege und Öffnung einer verstopften Nase. An der äußeren Nase wird die Austrocknung eher als Verkrustung und unangenehm empfunden. Dann schmiert man die Nasenöffnung mit Fettcreme ein.
In den Atemwegen scheint aber die Wärme sehr günstig zu wirken, da auch hartnäckiger chronischer Husten und die Verschleimung oft schon nach 2 Tagen deutlich besser werden.
Die Raumtemperatur sollte in so einem Fall im Wohlfühlbereich von 18 bis 22 Grad liegen und die Luftfeuchtigkeit bei 40 bis 60 %.
Entlassung
BearbeitenGut planen:
- LTOT/Beatmung für Zuhause notwendig?
Und nicht wundern, manchmal war es dann doch zu früh und die Patienten kommen bald wieder, vor allem bei schwerer COPD.
Weitere Tipps: https://www.atemwegsliga.de/tl_files/eigene-dateien/informationsmaterial/2020-%20Checkliste%20Entlassmanagement-COPD.pdf
Verlauf und Prognose
BearbeitenDie BODE-Skala bzw der BODE-Index korreliert mit der Letalität der ERkrankung und gibt Aufschluss über die statistische Lebenserwartung in Abhängigkeit des Schweregrads.
Verstorben
nach 24 Monaten nach 24 Monaten
Punktzahl
1-2 6% 19%
3-4 8% 32%
5-6 15% 43%
≥ 7 30% 76%
Errechnet wird der BODE-Index aus BMI, FEV1, mMRC und Gehstrecke im 6 min Gehtest
Punkte 0 1 2 3 BMI >21 ≤21 FEV1 (%d.S.) ≥65 ≥50 ≥36 ≤35 mMRC 0-1 2 3 4 6min Gehtest >350m ≥250m ≥150m ≤149m
Die Punktzahl der einzelnen Parameter wird addiert, Auswertung s.o.
Fälle
BearbeitenGeschichte der Krankheit
BearbeitenExperten und Krankenhäuser
BearbeitenSelbsthilfe
BearbeitenWas kann ich als Betroffener selber tun ?
BearbeitenSelbsthilfegruppen
BearbeitenPatientenratgeber
BearbeitenDie Patienten-Bibliothek gemeinnützige GmbH stellt allen interessierten Ärzten 4 x im Jahr eine kostenfreie Zeitschrift zum Bereich Atemwege zur Verfügung. Ca. 20 Patientenratgeber zu diesem Themenkomplex können bestellt werden, oder auch auf der eigenen Internetseite (PDF) für Patienten als Online-Ratgeber (kostenfrei) installiert werden. Kontakt/Bestellungen unter der Internetseite patienten-bibliothek.de