Einführung in die Allgemeine und die Anorganische Chemie: Zwischenmolekulare Kräfte
< Einführung in die Allgemeine und die Anorganische Chemie
Die zwischenmolekularen Kräfte werden auch Van der Waals-Kräfte genannt.
Sie entstehen durch Schwankungen in der Elektronenverteilung durch die Bewegung der Elektronen, die eine kurzzeitige partielle Teilladung in der Elektronenhülle und somit eine Polarisierung erzeugen.
Sie treten unter anderem bei Edelgasen, Halogenen, Molekülen (auch organischen) auf.
Weiterhin gibt es Wasserstoffbrückenbindungen. Hierbei gehen in Molekülen gebundene Atome wie N, O oder F eine zusätzliche schwache Bindung mit H-Atomen ein, z.B. beim Fluorwasserstoff:
H-F...H-F...H-F...H-F
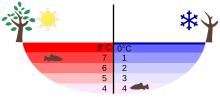
Die Formel H-F soll den Fluorwasserstoff darstellen, die ... ist die Wasserstoffbrückenbindung zwischen den freien Elektronen des Fluoratoms mit dem partiell negativ geladenen Wasserstoffatom eines benachbarten Fluorwasserstoffmoleküls. Dies ist auch beim Wasser der Fall, und sorgt dafür, dass die Wasseranomalie (die höchste Dichte (Masse pro Volumeneinheit) bei + 4°C bzw. dichteste Packung der Moleküle) auftritt. Erst durch diese Anomalie wird es möglich, dass Teiche und Seen von oben nach unten zufrieren, und dass Eis auf dem Wasser schwimmt.
Die Wasserstoffbrückenbindungen sorgen für höhere Siedepunkte als die bei den vorliegenden Verbindungen zu erwartenden Siedepunkte.
Die Struktur eines Schneekristalls wird auch durch die Wasserstoffbrückenbindungen beeinflusst: